[Năm 2022] Đề thi thử môn Hóa học THPT Quốc gia có lời giải (20 đề)
[Năm 2022] Đề thi thử môn Hóa học THPT Quốc gia có lời giải (20 đề) - Đề 8
-
3439 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 6:
Trong các chất sau, chất gây ô nhiễm không khí có nguồn gốc từ khí thải sinh hoạt là
 Xem đáp án
Xem đáp án
Chọn A
Câu 10:
Ở điều kiện thường, khí X không màu, không mùi, tan rất ít trong nước, không duy trì sự cháy và sự hô hấp. Trong không khí, khí X chiếm phần trăm thể tích lớn nhất. X là
 Xem đáp án
Xem đáp án
Chọn B
Câu 11:
Sắt(III) oxit được dùng để pha chế sơn chống gỉ. Công thức của Sắt(III) oxit là
 Xem đáp án
Xem đáp án
Chọn C
Câu 14:
Thể tích dung dịch H2SO4 0,5M cần dùng để trung hòa 100 ml dung dịch NaOH 0,5M là
 Xem đáp án
Xem đáp án
Chọn D
Câu 15:
Xà phòng hóa hoàn toàn 178 gam tristearin trong dung dịch KOH dư (đun nóng), thu được m gam kali stearat. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn D
Câu 17:
Cho các chất sau: metan, etilen, buta-1,3-đien, benzen, toluen, stiren, phenol và metyl acrylat. Số chất tác dụng được với nước brom ở điều kiện thường là
 Xem đáp án
Xem đáp án
Chọn A
Câu 19:
Tinh thể chất X và Y đều không màu, vị ngọt, dễ tan trong nước. Trong máu người có một lượng nhỏ chất X với nồng độ hầu như không đổi khoảng 0,1%. Y là đồng phân của X, có nhiều trong mật ong. Tên của X, Y lần lượt là
 Xem đáp án
Xem đáp án
Chọn B
Câu 21:
Cho hình vẽ dưới đây mô tả thí nghiệm điều chế khí Y từ dung dịch X.
Hình vẽ minh họa phản ứng nào sau đây?
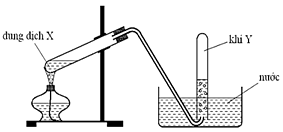
 Xem đáp án
Xem đáp án
Chọn A
Câu 22:
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư, thu được 8,96 lít khí. Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở điều kiện tiêu chuẩn. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn C
Câu 23:
Cho a mol sắt tác dụng với a mol khí clo, thu được hỗn hợp rắn X. Cho X vào nước, thu được dung dịch Y. Biết các phản ứng xảy ra hoàn toàn. Dung dịch Y không tác dụng với chất nào sau đây?
 Xem đáp án
Xem đáp án
Chọn D
Câu 24:
Đốt cháy hoàn toàn cacbohiđrat X, cần vừa đủ 5,6 lít O2 (đktc). Sản phẩm cháy thu được hấp thụ hoàn toàn vào 150 ml dung dịch Ba(OH)2 1M, thu được m gam kết tủa. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn B.
Khi đốt cacbohidrat ta có:
Hấp thụ CO2 vào 0,1 mol Ba(OH)2 thu được 2 muối
trong đó
Câu 25:
Tiến hành các thí nghiệm sau:
(a) Cho Na2O vào lượng nước dư.
(b) Điện phân dung dịch NaCl, điện cực trơ, có màng ngăn xốp.
(c) Cho dung dịch NaHSO4 vào dung dịch Ba(HCO3)2.
(d) Cho dung dịch NaHCO3 vào dung dịch Ca(OH)2 (tỉ lệ mol 1:1).
Số thí nghiệm thu được NaOH là
 Xem đáp án
Xem đáp án
Chọn B
Câu 27:
Hợp chất X có màu đỏ thẫm, tan rất tốt trong nước tạo thành dung dịch E chứa hỗn hợp hai axit (trong đó axit Y có tên gọi là axit đicromic). Cho dung dịch NaOH dư vào E, thu được dung dịch chứa chất Z có màu vàng. Thêm tiếp dung dịch H2SO4 loãng đến dư vào Z, thu được dung dịch chứa chất T có màu da cam. Các chất X, Y, Z, T lần lượt là
 Xem đáp án
Xem đáp án
Chọn B.
CrO3 (X) + H2O ® H2CrO4 (axit cromic) 2CrO3 + H2O ® H2Cr2O7 (Y) (axit đicromic)
2NaOH + H2CrO4 ® Na2CrO4 + 2H2O 4NaOH + H2Cr2O7 ® 2Na2CrO4 (Z)+ 3H2O
2Na2CrO4 + H2SO4 ® Na2Cr2O7 (T)+ Na2SO4 + H2O
Câu 28:
Hỗn hợp X gồm axetilen và etan có tỉ lệ mol tương ứng 1 : 2 qua ống đựng xúc tác thích hợp, nung nóng ở nhiệt độ cao thu được hỗn hợp Y gồm etan, etilen, axetilen và H2. Tỉ khối của hỗn hợp Y so với hidro là . Nếu cho 0,65 mol Y qua dung dịch Br2 dư thì số mol Br2 phản ứng tối đa là
 Xem đáp án
Xem đáp án
Chọn B.
Giả sử có 1 mol C2H2 và 2 mol C2H6 Þ mX = 86 (g) mà mX = mY Þ nY = 13/3
Ta có: = nY – nX = 4/3 mol
Vậy trong 0,65 mol Y có 0,5 mol brom tham gia phản ứng.
Câu 29:
Cho từ từ dung dịch HCl 1M vào dung dịch X chứa a mol NaHCO3 và b mol Na2CO3. Số mol khí CO2 thoát ra phụ thuộc vào thể tích HCl (ml) được biểu diễn ở đồ thị sau:
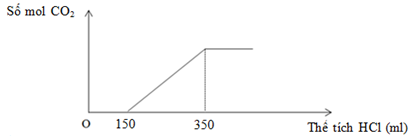
Tỉ lệ của a : b là
 Xem đáp án
Xem đáp án
Chọn D.
Các phản ứng xảy ra theo thứ tự:
(1) H+ + CO32- ® HCO3- (2) H+ + HCO3- ® CO2 + H2O
Tại V = 150 ml Þ nHCl = 0,15 mol thì
Tại V = 150 ml Þ nHCl = 0,35 mol thì
Vậy a : b = 4 : 3.
Câu 30:
Cho các phát biểu sau:
(a) Muối natri hoặc kali của axit béo được dùng để sản xuất xà phòng.
(b) Các amino axit thiên nhiên hầu hết là các α-amino axit.
(c) Trong phân tử fructozơ chỉ chứa một loại nhóm chức.
(d) Các polime sử dụng làm cao su được tổng hợp từ phản ứng trùng ngưng.
(e) Thành phần chính của cồn 75o mà trong y tế thường dùng để sát trùng là etanol.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn D.
(c) Sai, Trong phân tử fructozơ có chứa nhóm chức ancol (OH) và xeton (C=O).
(d) Sai, Các polime sử dụng làm cao su được tổng hợp từ phản ứng trùng hợp.
Câu 31:
Thực hiện chuỗi phản ứng sau (theo đúng tỉ lệ mol):
X (C7H10O6) + 3NaOH X1 + X2 + X3 + H2O
X1 + NaOH C2H6 + Na2CO3
X2 + H2SO4 → Y + Na2SO4
Y + 2CH3OH C4H6O4 + 2H2O
Biết X là hợp chất hữu cơ mạch hở và X3 tác dụng được với Na. Cho các phát biểu sau:
(a) Phân tử khối của Y là 90.
(b) X có mạch cacbon phân nhánh.
(c) Tên gọi của X1 là natri propionat.
(d) X3 hòa tan được Cu(OH)2 ở nhiệt độ thường.
(e) Từ etilen có thể điều chế trực tiếp X3 bằng một phản ứng.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn A.
(COOH)2 (Y) + 2CH3OH C4H6O4 + 2H2O
(COONa)2 (X2) + H2SO4 → (COOH)2 (Y) + Na2SO4
C2H5COONa (X1) + NaOH C2H6 + Na2CO3
Vậy X là HOOC-COO-C2H4-OOC-C2H5 Þ X3 là C2H4(OH)2 (vì X3 tác dụng được với Na)
(b) Sai. X có mạch cacbon không phân nhánh.
Câu 32:
Thực hiện các thí nghiệm sau:
(a) Cho dung dịch HCl vào dung dịch Fe(NO3)2.
(b) Cho FeS vào dung dịch HCl.
(c) Nhiệt phân muối K2CO3.
(d) Cho Fe vào dung dịch NaHSO4.
(e) Cho kim loại Al vào dung dịch FeCl2.
Số thí nghiệm có xảy ra phản ứng là
 Xem đáp án
Xem đáp án
Chọn A.
(a)
(b) FeS + 2HCl FeCl2 + H2S
(c) CrCl3 + 3NaOH ® Cr(OH)3 + 3NaCl
(d) Không xảy ra.
(e) Fe + 2NaHSO4 ® FeSO4 + Na2SO4 + H2
(g) 2Al + 3FeCl2 ® 2AlCl3 + 3Fe.
Câu 33:
Cho 18,81 gam hỗn hợp E chứa một este đơn chức X (chứa một liên kết C=C) và một axit đơn chức Y tác dụng vừa đủ với dung dịch NaOH, kết thúc phản ứng thu được ancol metylic và m gam một muối duy nhất. Mặt khác, đốt cháy hoàn toàn 0,16 mol E, thu được 122a gam CO2 và 39a gam H2O. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn C.
Vì thu được 1 muối duy nhất nên X và Y đều có k = 2
Khi đốt E ta có:
Þ X là C3H5COOCH3 và Y là C3H5COOH
Trong 18,81 gam có 0,2 mol E Þ Muối thu được là C3H5COONa: 0,2 mol có m = 21,6 (g)
Câu 34:
Đốt cháy hoàn toàn m gam triglixerit X (trung hòa) cần dùng 69,44 lít khí O2 (đktc) thu được khí CO2 và 36,72 gam nước. Đun nóng m gam X trong 150 ml dung dịch NaOH 1M, sau khi phản ứng xảy ra hoàn toàn thu được dung dịch Y. Cô cạn dung dịch Y thu được p gam chất rắn khan. Biết m gam X tác dụng vừa đủ với 12,8 gam Br2 trong dung dịch. Giá trị của p là
 Xem đáp án
Xem đáp án
Chọn B.
Ta có:
Khi cho X tác dụng với NaOH thì:
Câu 35:
Hấp thụ hoàn toàn V lít CO2 vào 200 ml dung dịch NaOH aM thì thu được dung dịch X. Cho từ từ 150 ml dung dịch HCl 0,5M vào X và khuấy đều, thu được dung dịch Y và 1,12 lít khí. Cho Y tác dụng với Ca(OH)2 dư xuất hiện 7,5 gam kết tủa. Giá trị của a là
 Xem đáp án
Xem đáp án
Chọn B.
Khi cho Y tác dụng với Ca(OH)2 thì thu được 0,075 mol CaCO3
Dung dịch Y chứa Na+ (0,2a mol), Cl- (0,075 mol), HCO3- (0,075 mol)
Câu 36:
Hòa tan hoàn toàn hai chất rắn X, Y (có số mol bằng nhau) vào nước, thu được dung dịch Z.
Tiến hành các thí nghiệm sau:
Thí nghiệm 1: Cho dung dịch Ba(OH)2 dư vào V ml dung dịch Z, thu được n1 mol kết tủa.
Thí nghiệm 2: Cho dung dịch NH3 dư vào V ml dung dịch Z, thu được n2 mol kết tủa.
Thí nghiệm 3: Cho dung dịch H2SO4 loãng, dư vào V ml dung dịch Z, thu được n3 mol khí NO (sản phẩm khử duy nhất của N+5).
Biết các phản ứng xảy ra hoàn toàn và n3 < n1 < n2. Hai chất X, Y lần lượt là
 Xem đáp án
Xem đáp án
Chọn A.
Dựa vào các đáp án ta thấy trường hợp của Al(NO3)3, Fe(NO3)2 thỏa mãn n3 < n1 < n2 vì:
+ Thí nghiệm 1:
+ Thí nghiệm 2:
+ Thí nghiệm 3:
Câu 37:
Hỗn hợp X gồm các chất hữu cơ có cùng công thức phân tử là C2H8O3N2. Cho m gam X phản ứng vừa đủ với dung dịch NaOH đun nóng, thu được dung dịch Y chỉ gồm các chất vô cơ và 6,72 lít (đktc) hỗn hợp Z gồm 3 amin. Cô cạn dung dịch Y, thu được 29,28 gam hỗn hợp muối khan. Mặt khác, cho m gam X phản ứng hoàn toàn với dung dịch HCl thì thu được V lít khí (đktc). Giá trị của V là
 Xem đáp án
Xem đáp án
Chọn B.
X gồm các đồng phân: C2H5NH3NO3; (CH3)2NH2NO3; CH2(NH3)2CO3 và H2NCH2NH3HCO3
Đặt số mol 2 chất đầu là a mol và 2 chất sau là b mol Þ a + b = 0,3 (1)
Muối thu được gồm NaNO3 (a mol) và Na2CO3 (b mol) Þ 85a + 106b = 29,28 (2)
Từ (1), (2) suy ra: a = 0,12 ; b = 0,18
Khi cho X tác dụng với HCl thu được khí CO2 (b = 0,18 mol) Þ V = 4,032 (l).
Câu 38:
Hình vẽ mô tả quá trình điều chế khí metan trong phòng thí nghiệm:
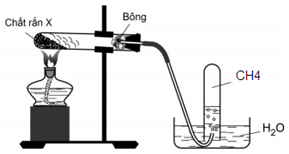
Một học sinh dựa vào thí nghiệm trên đã nêu ra các phát biểu sau:
(a) Khí metan dễ tan trong nước nên cần phải thu bằng phương pháp đẩy nước.
(b) Các chất rắn trong X là CaO, NaOH, CH3COONa.
(c) Ống nghiệm đựng chất rắn khi lắp cần phải cho miệng hơi chúc xuống dưới.
(d) Khi kết thúc thí nghiệm phải tắt đèn cồn trước rồi mới tháo ống dẫn khí.
(e) CaO là chất bảo vệ ống thủy tinh, tránh bị nóng chảy.
Số phát biểu đúng trong các phát biểu trên là
 Xem đáp án
Xem đáp án
Chọn A.
(a) Sai, Khí metan không tan trong nước nên cần phải thu bằng phương pháp đẩy nước.
(d) Sai, Khi kết thúc thí nghiệm phải tháo ống dẫn khí trước rồi mới tắt đèn cồn.
(e) Sai, Mục đích của việc dùng vôi (CaO) trộn với xút (NaOH) là để ngăn không cho NaOH làm thủng ống nghiệm dẫn đến nguy hiểm.
Câu 39:
Hòa tan hoàn toàn 22,92 gam hỗn hợp gồm FeCO3 và Cu trong 110 gam dung dịch HNO3 50,4% thu được m gam dung dịch X và V lít (đktc) hỗn hợp hai khí không màu (trong đó có một khí hóa nâu trong không khí là sản phẩm khử duy nhất của N+5). Cho 400 ml dung dịch KOH 2M vào X thu được kết tủa Y và dung dịch Z. Cô cạn Z, sau đó đem nung đến khối lượng không đổi thu được 65,68 gam rắn khan. Các phản ứng xảy ra hoàn toàn. Giả sử nước bay hơi không đáng kể. Nồng độ phần trong của Fe(NO3)3 trong dung dịch X gần nhất với giá trị?
 Xem đáp án
Xem đáp án
Chọn D.
Chất rắn thu được gồm KOH (x mol) và KNO2 (y mol)
Giả sử trong X chỉ chứa muối Fe3+ và Cu2+ Þ (vô lí)
Vậy trong X có H+ dư vì vậy ta có thể xác định rằng là muối thu được là Fe3+ và Cu2+.
Đặt FeCO3 (a mol) và Cu (b mol) Þ
Khối lượng dung dịch X: 22,92 + 110 – 0,16.30 – 0,09.44 = 124,16 (g) Þ
Câu 40:
Cho hai axit cacboxylic X, Y đều đơn chức, mạch hở (trong phân tử X, Y chứa không quá hai liên kết p và 46 < MX < MY); Z là trieste được tạo bởi X, Y và glixerol. Đốt cháy 13,36 gam hỗn hợp E chứa X, Y và Z cần dùng 0,52 mol O2. Mặt khác, 0,32 mol E làm mất màu tối đa 0,1 mol Br2 trong dung dịch. Cho 20,04 gam E tác dụng vừa đủ với 300 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng, thu được hỗn hợp F gồm hai muối F1 và F2 (). Phần trăm khối lượng của F1 trong F gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Chọn A.
Ta có 20,04 : 13,36 = 1,5 Þ Trong 13,36 gam E thì có 0,2 mol NaOH phản ứng.
Đặt x, y là số mol của X, Y và z là số mol của Z Þ x + y + 3z = 0,2 (1)
Khi đốt cháy E thì:
Vì tỉ lệ nên trong E có Y là axit không no chứa 1 liên kết C=C; còn X là axit no và Z tạo bởi X, Y trong đó có 1 liên kết C=C (chứa 2 gốc X và 1 gốc Y)
Dựa vào độ bất bão hòa:
Từ (1), (2), (3) suy ra: x = 0,11 ; y = 0,03 ; z = 0,02
Trong 20,04 gam E có chứa muối F1 là CH3COONa: 1,5.(0,02.2 + 0,11) = 0,225 mol và C2H3COONa 1,5.(0,02 + 0,03) = 0,075 mol Þ
