Bộ đề thi thử môn Hóa THPT Quốc gia năm 2022 có lời giải (30 đề)
Bộ đề thi thử THPT Quốc gia năm 2022 môn Hóa có lời giải (Đề 23)
-
5179 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 3:
Sục khí CO2 vào lượng dư dung dịch nào sau đây sẽ thu được kết tủa?
 Xem đáp án
Xem đáp án
Câu 4:
Đốt cháy hiđrocacbon nào sau đây thu được số mol H2O nhỏ hơn số mol CO2
 Xem đáp án
Xem đáp án
Câu 5:
PVC là chất rắn vô định hình, cách điện tốt, bền với axit, được dùng làm vật liệu cách điện, ống dẫn nước, vải che mưa,... PVC được tổng hợp trực tiếp từ monome nào sau đây?
 Xem đáp án
Xem đáp án
Câu 9:
Để đề phòng bị nhiểm độc CO, người ta sử dụng mặt nạ phòng độc có chứa hóa chất nào sau đây?
 Xem đáp án
Xem đáp án
Câu 11:
Trong các trường hợp sau, trường hợp nào không xảy ra ăn mòn điện hoá?
 Xem đáp án
Xem đáp án
Câu 13:
Kim loại nào sau đây hiện nay được điều chế chủ yếu bằng phương pháp nhiệt luyện?
 Xem đáp án
Xem đáp án
Câu 15:
Hòa tan hết 6,5 gam Zn trong dung dịch HCl dư thu được V lít H2 (đktc). Giá trị của V là
 Xem đáp án
Xem đáp án
Câu 16:
Kim loại khác nhau có độ dẫn điện, dẫn nhiệt khác nhau. Sự khác nhau đó được quyết định bởi.
 Xem đáp án
Xem đáp án
Câu 17:
Một peptit X mạch hở khi thuỷ phân hoàn toàn chỉ thu được glyxin. Khi đốt cháy 0,1 mol X thu được 12,6 gam nước. Số nguyên tử oxi có trong 1 phân tử X là
 Xem đáp án
Xem đáp án
Chọn D.
Số
Peptit có k mắt xích Gly
Số
Câu 18:
Hòa tan Fe3O4 vào dung dịch H2SO4 loãng dư, thu được dung dịch X. Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
Chọn C.
A. Đúng:
B. Đúng, thu được
C. Sai, X có hòa tan Cu vì:
D. Đúng:
Câu 19:
Cho vào ống nghiệm khô có nút cao su và ống dẫn khí khoảng 4 - 5 gam hỗn hợp bột mịn (X) đã được trộn đều gồm natri axetat khan và vôi tôi xút theo tỉ lệ 1 : 2 về khối lượng. Lắp dụng cụ như hình vẽ sau:
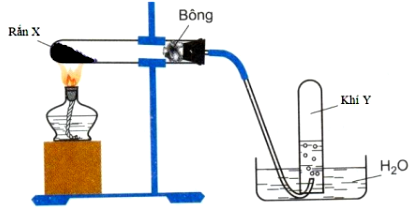
Khí Y được điều chế trong thí nghiệm trên là
 Xem đáp án
Xem đáp án
Chọn A.
Khí Y là
Câu 20:
Hiệu ứng nhà kính là hiện tượng Trái Đất đang ấm dần lên do các bức xạ có bước sóng dài trong vùng hồng ngoại bị giữ lại mà không bức xạ ra ngoài vũ trụ. Khí nào dưới đây là nguyên nhân chính gây ra hiệu ứng nhà kính?
 Xem đáp án
Xem đáp án
Câu 21:
Khi đun nóng chất X có công thức phân tử C3H6O2 với dung dịch NaOH thu được CH3COONa. Công thức cấu tạo của X là
 Xem đáp án
Xem đáp án
Câu 22:
Thuỷ phân 62,5 gam dung dịch saccarozơ 17,1% trong môi trường axit (vừa đủ) được dung dịch X. Cho dung dịch AgNO3/NH3 vào X và đun nhẹ được m gam Ag. (biết các phản ứng xảy ra hoàn toàn) Giá trị của m là?
 Xem đáp án
Xem đáp án
Chọn A.
Câu 23:
Mô tả hiện tượng nào sau đây không chính xác?
 Xem đáp án
Xem đáp án
Câu 24:
Thủy phân hoàn toàn 8,8 gam CH3COOC2H5 trong 100 ml dung dịch KOH 1,5M, đun nóng. Sau phản ứng hoàn toàn, cô cạn dung dịch thu được m gam chất rắn khan. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn D.
và
Chất rắn gồm và KOH dư (0,05)
m rắn = 12,6 gam
Câu 25:
Cho 2,00 gam một kim loại M thuộc nhóm IIA tác dụng hết với dung dịch HCl tạo ra 5,55 gam muối. Kim loại M là
 Xem đáp án
Xem đáp án
Chọn B.
M là Ca
Câu 26:
Cho 11,6 gam Fe vào 100 ml dung dịch CuSO4 1M. Sau khi phản ứng xảy ra hoàn toàn, thu được m gam hỗn hợp kim loại. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn D.
nên bị khử hết.
gam
Câu 27:
Cho các polime sau: polietilen; xenlulozơ; polipeptit; tinh bột; tơ nilon-6; tơ nilon-6,6; polibutađien. Dãy các polime tổng hợp là
 Xem đáp án
Xem đáp án
Câu 28:
Trung hòa dung dịch chứa 7,08 gam amin X no, đơn chức mạch hở cần dùng 120 ml dung dịch H2SO4 0,5M. Số công thức cấu tạo của X là
 Xem đáp án
Xem đáp án
Chọn D.
X là
X có 4 cấu tạo:
Câu 29:
Hòa tan hoàn toàn 5,95 gam hỗn hợp hai kim loại Al và Zn bằng dung dịch H2SO4 loãng (vừa đủ) thì thu được dung dịch X có khối lượng tăng 5,55 gam. Cô cạn dung dịch X, thu được muối khan có khối lượng?
 Xem đáp án
Xem đáp án
Chọn D.
Đặt a, b là số mol
và
gam
gam
m muối gam
Câu 30:
Cho từ từ dung dịch HCl vào dung dịch chứa a mol Na2CO3 và b mol NaHCO3. Số mol khí CO2 thu được phụ thuộc vào số mol HCl được biểu diễn theo đồ thị dưới đây:
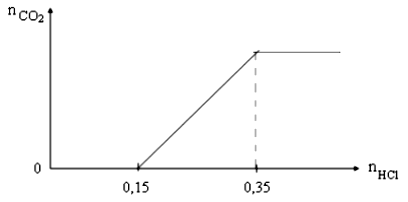
Tỉ lệ của a : b bằng
 Xem đáp án
Xem đáp án
Chọn D.
Câu 31:
Hỗn hợp X gồm axit oleic và triglixerit Y. Đốt cháy hoàn toàn 0,2 mol X cần vừa đủ 10,6 mol O2, thu được CO2 và 126 gam H2O. Mặt khác, cho 0,12 mol X tác dụng với dung dịch NaOH vừa đủ, đun nóng, thu được glixerol và x gam hỗn hợp gồm natri oleat và natri stearat. Giá trị của x là
 Xem đáp án
Xem đáp án
Chọn D.
Quy đổi X thành và
Muối gồm và
m muối = 121,8
Tỉ lệ: 0,2 mol X tạo 121,8 gam muối
Từ 0,12 mol X tạo m muối = 73,08 gam
Câu 32:
Dẫn khí CO dư qua ống sứ đựng 16 gam bột Fe2O3 nung nóng, thu được hỗn hợp khí X. Cho toàn bộ X vào nước vôi trong dư, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn D.
dư
gam.
Câu 33:
Cho hỗn hợp gồm Na và Al có tỉ lệ số mol tương ứng là 1 : 2 vào nước (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H2 (ở đktc) và m gam chất rắn không tan. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn B.
Đặt a, 2a là số mol Na và Al
pư
dư gam.
Câu 34:
Cho 0,15 mol axit glutamic vào 175 ml dung dịch HCl 2M, thu được dung dịch X. Cho dung dịch NaOH dư vào X. Sau khi phản ứng xảy ra hoàn toàn, số mol NaOH tham gia phản ứng là
 Xem đáp án
Xem đáp án
Chọn A.
Dung dịch chứa:
mol
mol
Bảo toàn điện tích mol
Vậy
Câu 35:
Điều chế este CH3COOC2H5 trong phòng thí nghiệm được mô tả theo hình vẽ dưới đây:
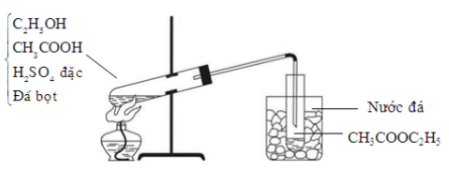
Cho các phát biểu sau:
(a) Etyl axetat có nhiệt độ sôi thấp (77°C) nên dễ bị bay hơi khi đun nóng.
(b) H2SO4 đặc vừa làm chất xúc tác, vừa có tác dụng hút nước.
(c) Etyl axetat qua ống dẫn dưới dạng hơi nên cần làm lạnh bằng nước đá để ngưng tụ.
(d) Khi kết thúc thí nghiệm, cần tắt đèn cồn trước khi tháo ống dẫn hơi etyl axetat.
(e) Vai trò của đá bọt là để bảo vệ ống nghiệm không bị vỡ.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn C.
(a) Đúng
(b) Đúng
(c) Đúng
(d) Đúng, tắt đèn cồn trước khi tháo ống dẫn khí để tránh hơi este chưa thoát ra hết bắt lửa cháy.
(e) Sai, đá bọt giúp hỗn hợp chất lỏng sôi êm dịu.
(g) Sai, do hỗn hợp phản ứng chứa H2SO4 nên không dùng CaCO3 làm đá bọt, phải chọn 1 chất trơ để làm đá bọt, ở đây có thể dùng vụn thủy tin, vụn gạch…
Câu 36:
Cho các phát biểu sau:
(a) Xenlulozơ thuộc loại polime thiên nhiên.
(b) Muối natri hoặc kali của axit béo được dùng để sản xuất xà phòng.
(c) Để giảm đau nhức khi bị kiến đốt, có thể bôi vôi tôi vào vết đốt.
(d) Sau khi mổ cá, có thể dùng giấm ăn để giảm mùi tanh.
(e) Các hợp chất peptit kém bền trong môi trường bazơ nhưng bền trong môi trường axit.
Số lượng phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn B.
(a) Đúng
(b) Đúng
(c) Đúng, nọc kiến chứa HCOOH, vôi tôi sẽ trung hòa axit này làm giảm đau, ngứa.
(d) Đúng, mùi tanh gây ra bởi một số amin, giấm ăn sẽ chuyển amin thành dạng muối dễ bị rửa trôi.
(e) Sai, kém bền trong cả axit và bazơ
Câu 37:
Hỗn hợp E gồm amino axit X, đipeptit Y (C4H8O3N2) và muối của axit vô cơ Z (C2H8O3N2). Cho E tác dụng với 200 ml dung dịch NaOH 1,5M và KOH 1M đun nóng (phản ứng vừa đủ), thu được 4,48 lít khí T (đo ở đktc, phân tử T có chứa một nguyên tử nitơ và làm xanh quỳ tím ẩm). Cô cạn dung dịch sau phản ứng, thu được m gam chất rắn khan gồm bốn muối. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn B.
Bốn muối (2 muối natri + 2 muối kali) Chỉ có 2 gốc axit.
X là Gly: Y là Gly-Gly và Z là
Muối chứa các icon: bảo toàn điện tích
m muối = 49,3 gam.
Câu 38:
Chất hữu cơ X mạch hở có công thức phân tử C8H12O4 và thỏa sơ đồ các phản ứng sau:
(a) X + 2NaOH → Y + Z + T
(b) X + H2 → E
(c) E + 2NaOH → 2Y + T
(d) Y + HCl → NaCl + F
Khẳng định nào sau đây đúng?
 Xem đáp án
Xem đáp án
Chọn A.
và Sau khi cộng thì Z chuyển thành Y, vậy Z có 1 nối đôi cùng C và ít nhất 3C.
là muối của axit đơn chức
Phát biểu B đúng:
Câu 39:
Hòa tan hết a gam bột Fe trong 100 ml dung dịch HCl 1,2M, thu được dung dịch X và 0,896 lít khí H2. Cho X tác dụng với lượng dư dung dịch AgNO3, sau khi kết thúc các phản ứng thu được V lít khí NO (sản phẩm khử duy nhất) và b gam chất rắn, (biết các khí đo ở đktc). Giá trị của b và V lần lượt là:
 Xem đáp án
Xem đáp án
Chọn D.
Bảo toàn dư = 0,04
lít
Bảo toàn electron:
Bảo toàn
gam.
Câu 40:
Cho X, Y là hai chất thuộc dãy đồng đẳng của axit acrylic và MX < MY; Z là ancol có cùng số nguyên tử cacbon với X; T là este hai chức tạo bởi X, Y và Z. Đốt cháy hoàn toàn 11,16 gam hỗn hợp E gồm X, Y, Z, T cần vừa đủ 13,216 lít khí O2 (đktc), thu được khí CO2 và 9,36 gam nước. Mặt khác 11,16 gam E tác dụng tối đa với dung dịch chứa 0,04 mol Br2. Khối lượng muối thu được khi cho cùng lượng E trên tác dụng hết với dung dịch KOH dư là
 Xem đáp án
Xem đáp án
Chọn A.
Bảo toàn khối lượng
Do nên ancol no.
Quy đổi X thành và
Do nên ancol không chứa thêm Axit gồm và
Muối gồm và m muối = 4,68 gam.
