20 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án
20 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án ( Đề 11)
-
3324 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Oxit nào sau đây là không phải oxit axit?
 Xem đáp án
Xem đáp án
P2O5, CrO3, CO2 là oxit axit. Cr2O3 là oxit lưỡng tính.
Chọn đáp án D.
Câu 2:
Người ta thường bảo quản kim loại kiềm bằng cách nào sau đây?
 Xem đáp án
Xem đáp án
Các kim loại kiềm có tính khử rất mạnh, dễ bị oxi hóa bởi nước. Để bảo quản, người ta thường ngâm các kim loại kiềm trong dầu hỏa.
Chọn đáp án D.
Câu 3:
Công thức phân tử và công thức cấu tạo của xenlulozơ lần lượt là:
 Xem đáp án
Xem đáp án
Công thức phân tử và công thức cấu tạo của xenlulozơ lần lượt là: (C6H10O5)n và [C6H7O2(OH)3]n.
Chọn đáp án B.
Câu 4:
Polime nào sau đây có cấu trúc mạch phân nhánh?
 Xem đáp án
Xem đáp án
Amilopectin là polime có cấu trúc mạch phân nhánh.
Chọn đáp án A.
Câu 5:
X là một hợp chất hữu cơ có khả năng làm quỳ tím chuyển xanh và có công thức cấu tạo: . Tên gọi của X là?
 Xem đáp án
Xem đáp án
X là một amino axit, có khả năng làm quỳ tím chuyển xanh vì trong công thức cấu tạo: số nhóm > số nhóm . Tên gọi của X là lysin.
Chọn đáp án D.
Câu 6:
Trong các chất dưới đây, chất nào có lực bazơ yếu nhất?
 Xem đáp án
Xem đáp án
Xét các công thức mà đề bài cho, do trong công thức cấu tạo của (C6H5)2NH có 2 nhóm là nhóm hút electron (C6H5)2NH là chất có lực bazơ yếu nhất.
Chọn đáp án A.
Câu 7:
Trong công nghiệp, có thể chuyển hóa trực tiếp từ chất bẻo lỏng sang chất béo rắn bằng phản ứng
 Xem đáp án
Xem đáp án
Trong công nghiệp, có thể chuyển hóa trực tiếp từ chất béo lỏng thành chất béo rắn bằng phản ứng hiđro hóa có xúc tác Ni.
VD:
Chọn đáp án B.
Câu 8:
Propyl axetat có công thức là?
 Xem đáp án
Xem đáp án
Propyl axetat có công thức là: CH3COOCH2CH2CH3.
Chọn đáp án C.
Câu 9:
Người ta thường dùng cát làm khuôn đúc kim loại. Để làm sạch hoàn toàn những hạt cát bám trên bề mặt vật dụng làm bằng kim loại có thể dùng dung dịch nào sau đây?
 Xem đáp án
Xem đáp án
Axit HF có thể hòa tan được SiO2 theo phương trình phản ứng sau:
Chọn đáp án B.
Câu 10:
Kim loại X tác dụng với H2SO4 loãng giải phóng khí H2. Mặt khác, oxit của X bị H2 khử thành kim loại ở nhiệt độ cao. X là kim loại nào?
 Xem đáp án
Xem đáp án
Kim loại X tác dụng với H2SO4 loãng giải phóng khí H2 X có thể là: Fe, Al, Mg. Oxit của X bị H2 khử thành kim loại ở nhiệt độ cao X là: Fe.
Chọn đáp án A.
Câu 11:
Phát biểu nào sau đây là đúng?
 Xem đáp án
Xem đáp án
A. Sai, nitrophotka là hỗn hợp của KNO3 vàọ (NH4)2HPO4.
B. Đúng.
C. Sai, supephotphat đơn là hỗn hợp của Ca(H2PO4)2 và CaSO4.
D. Sai, phân đạm ure là (NH2)2CO.
Chọn đáp án B.
Câu 12:
Cho các chất: stiren, benzen, propilen, axetilen. Số chất làm mất màu nước brom ở nhiệt đồ thường là?
 Xem đáp án
Xem đáp án
Các hiđrocacbon có liên kết bội (trừ liên kết trong vòng benzen) đều làm mất màu nước brom. Các hiđrocacbon thỏa mãn là: stiren, propilen, axetilen.
Chọn đáp án C.
Câu 14:
Nếu quy định nồng độ tối đa cho phép của Pb2+ trong nước sinh hoạt là 0,05 mg/l. Hãy cho biết nguồn nước nào dưới đây bị ô nhiễm nặng bởi Pb2+?
 Xem đáp án
Xem đáp án
A. Nồng độ
B. Nồng độ
C. Nồng độ
D. Nồng độ
Chọn đáp án C.
Câu 15:
Số mắt xích glucozơ có trong 194,4 mg amilozơ là (cho biết số Avogađro ):
 Xem đáp án
Xem đáp án
Amilozơ là polime có cấu trúc mạch không phân nhánh, do nhiều mắt xích -glucozơ liên kết với nhau tạo thành.
Số mắt xích
.
Chọn đáp án D.
Câu 16:
Một -aminoaxit X no chỉ chứa 1 nhóm -NH2 và 1 nhóm -COOH. Cho 17,8 gam X tác dụng với dung dịch HCl dư thu được 25,1 gam muối. Tên gọi của X là:
 Xem đáp án
Xem đáp án
Bản chất của phản ứng là:
(1)
Áp dụng định luật bảo toàn khối lượng ta có:
Vì X là một -aminoaxit no chỉ chứa 1 nhóm và 1 nhóm nên suy ra:
.
Đặt công thức phân tử của X là H2NRCOOH, 16 + R + 45 = 89 R = 28.
Do X là -aminoaxit nên công thức cấu tạo của X là CH3CH(NH2)COOH.
Tên gọi của X là axit -aminopropionic.
Chọn đáp án D.
Câu 17:
Hòa tan hoàn toàn m1 gam FeSO4.7H2O vào m2 gam dung dịch FeSO4 10,16% để thu được dung dịch FeSO4 25%. Tỉ lệ là
 Xem đáp án
Xem đáp án
coi FeSO4.7H2O là dung dịch FeSO4 có nồng độ phần trăm là:
.
Áp dụng sơ đồ đường chéo ta có:
Chọn đáp án A.
Câu 18:
Hiđro hóa hoàn toàn 20 gam hỗn hợp X gồm 3 ankađien thu được 20,8g hỗn hợp ankan. Hãy cho biết 20 gam hỗn hợp X làm mất màu vừa hết bao nhiêu gam dung dịch Br2 32%?
 Xem đáp án
Xem đáp án
Gọi CTTQ 3 ankađien là: CnH2n-2 ( ):
§ Khối lượng bình tăng
.
§ Để phản ứng vừa hết với .
§ Dung dịch Brom có .
Chọn đáp án C.
Câu 19:
Thủy phân hoàn toàn 55,95 gam một peptit X thu được 66,75 gam alanin (amino axit duy nhất). X là:
 Xem đáp án
Xem đáp án
Để phản ứng hết với các muối KHCO3 và K2CO3 thì lượng HCl cần dùng là:
HCl thiếu, lượng CO2 tính theo HCl.
Theo giả thiết ta có:
Do đó ta gọi số mol của các ion và tham gia phản ứng là 2x và x.
Khi cho từ từ dung dịch chứa các ion và vào dung dịch chứa ion thì phản ứng xảy ra đồng thời (1) và (2).
Tổng số mol H+ là: lít.
Chọn đáp án B.
Câu 20:
Thủy phân hoàn toàn 55,95 gam một peptit X thu được 66,75 gam alanin (amino axit duy nhất). X là:
 Xem đáp án
Xem đáp án
Theo đầu bài ta có:
Sơ đồ phản ứng thủy phân:
Theo (1) và giả thiết ta có: Vậy X là pentapeptit.
Chọn đáp án C.
Câu 21:
Thủy phân hoàn toàn 444 gam một lipit thu được 46 gam glixerol và hai loại axit béo. Xác định công thức của hai loại axit béo trên.
 Xem đáp án
Xem đáp án
Đặt công thức trung bình của lipit là .
Phản ứng hóa học:
Như vật trong lipit phải có ít nhất một gốc là C17H35 (239).
Nếu lipit có công thức là RCOOC3H5(OOCC17H35)2 thì .
Nếu lipit có công thức là (RCOO)2C3H5OOCC17H35 thì (loại).
Chọn đáp án B.
Câu 22:
Este X mạch hở được tạo ra từ axit no A và etylen glicol. Biết rằng a gam X ở thể hơi chiếm thể tích bằng thể tích của 6,4 gam oxi ở cùng điều kiện nhiệt độ và áp suất; Mặt khác, a gam X phản ứng hết với xút tạo ra 32,8 gam muối. Nếu cho 200 gam A phản ứng với 50 gam etylen glicol ta thu được 87,6 gam este. Tên của X và hiệu suất phản ứng tạo X là:
 Xem đáp án
Xem đáp án
Đặt công thức của este X là C2H4(OOCR)2;
Phương trình phản ứng:
Theo (1) và giả thiết suy ra: R là .
Phương trình phản ứng tổng hợp este X:
Căn cứ vào tỉ lệ mol trên phương trình (2) suy ra axit dư, hiệu suất phản ứng tính theo ancol. Theo (2) số mol ancol phản ứng là 0,6 mol nên hiệu suất phản ứng là
.
Chọn đáp án A.
Câu 23:
Cho m gam hỗn hợp bột X gồm ba kim loại Zn, Cr, Sn có số mol bằng nhau tác dụng hết với lượng dư dung dịch HCl loãng, nóng thu được dung dịch Y và khí H2. Cô cạn dung dịch Y thu được 8,98 gam muối khan. Nếu cho m gam hỗn hợp X tác dụng hoàn toàn với O2 (dư) để tạo hỗn hợp 3 oxit thì thể tích khí O2 (đktc) phản ứng là:
 Xem đáp án
Xem đáp án
Theo đầu bài ta có:
Chọn đáp án D.
Câu 24:
Thủy phân hoàn toàn 6,84 gam saccarozơ rồi chia sản phẩm thành 2 phần bằng nhau. Phần 1 cho tác dụng với lượng dư dung dịch AgNO3/NH3 thì thu được x gam kết tủa. Phần 2 cho tác dụng với dung dịch nước brom dư, thì có y gam brom tham gia phản ứng. Giá trị x và y lần lượt là:
 Xem đáp án
Xem đáp án
Theo đầu bài ta có:
Phương trình phản ứng thủy phân:
Phần 1: Khi thực hiện phản ứng tráng gương thì cả glucozơ và fructozơ đều tham gia phản ứng tổng số mol phản ứng là 0,02 mol.
Phần 2: Khi phản ứng với dung dịch nước brom thì chỉ có glucozơ phản ứng.
Vậy từ (2) và (3) suy ra:
Chọn đáp án C.
Câu 25:
Lấy 0,3 mol hỗn hợp X gồm H2NC3H5(COOH)2 và H2NCH2COOH cho vào 400 ml dung dịch HCl 1M thì thu được dung dịch Y. Y tác dụng vừa đủ với 800 ml dung dịch NaOH 1M thu được dung dịch Z. Làm bay hơi Z thu được m gm chất rắn khan, giá trị của m là:
 Xem đáp án
Xem đáp án
Bản chất của các phản ứng:
Theo (1), (2) và giả thiết suy ra số mol nhóm là 0,4 mol.
Gọi số mol của H2NC3H5(COOH)2 và H2NCH2COOH là x và y ta có hệ:
Áp dụng định luật bảo toàn khối lượng ta có:
.
Câu 26:
Hỗn hợp X gồm alanin, axit glutamic và axit acrylic. Hỗn hợp Y gồm propen và trimetylamin. Đốt cháy hoàn toàn a mol X và b mol Y thì tổng hợp mol oxi cần dùng vừa đủ là 1,14 mol, thu được H2O; 0,1 mol N2 và 0,91 mol CO2. Mặt khác, khi cho a mol X tác dụng với dung dịch KOH dư thì lượng KOH phản ứng là m gam. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
 Xem đáp án
Xem đáp án
Quy đổi X, Y thành
Khối lượng KOH .
Chọn đáp án A.
Câu 27:
Thổi khí CO2 vào dung dịch chứa 0,02 mol Ba(OH)2. Giá trị khối lượng kết tủa biến thiên trong khoảng nào khi CO2 biến thiên trong khoảng từ 0,005 mol đến 0,024 mol?
 Xem đáp án
Xem đáp án
Khi số mol CO2 biến thiên trong khoảng (0,005; 0,024) và mol Ba(OH)2 là 0,02 mol thì lượng kết tủa lớn nhất thu được là khi .
Từ (1) .
Khi số mol CO2 là 0,005 mol
Khi số mol CO2 là 0,02 mol = mol Ba(OH)2 thì kết tủa đạt max = 3,94 gam.
Khi số mol CO2 là 0,024 mol > 0,02 mol thì lượng kết tủa max đã bị hòa tan 1 phần.
Khối lượng kết tủa biến đổi trong đoạn từ 0,985 gam đến 3,94 gam.
Chọn đáp án A.
Câu 28:
Tiến hành các thí nghiệm sau:
(a) Đốt dây sắt trong bình chứa khí Cl2.
(b) Nung nóng hỗn hợp bột gồm Fe và S (trong khí trơ).
(c) Cho bột Cu (dư) vào dung dịch FeCl3.
(d) Cho Fe(NO3)2 vào dung dịch HCl.
(e) Cho Fe vào dung dịch AgNO3 (dư).
Sau các phản ứng, số thí nghiệm tạo ra muối sắt (III) là
 Xem đáp án
Xem đáp án
Các phản ứng xảy ra:
(a)
(b)
(c)
(d)
(e)
Các thí nghiệm tạo ra muối sắt (III) là (a), (d), (e).
Chọn đáp án B.
Câu 29:
Cho hình vẽ mô tả thí nghiệm điều chế chất lỏng Y từ dung dịch X
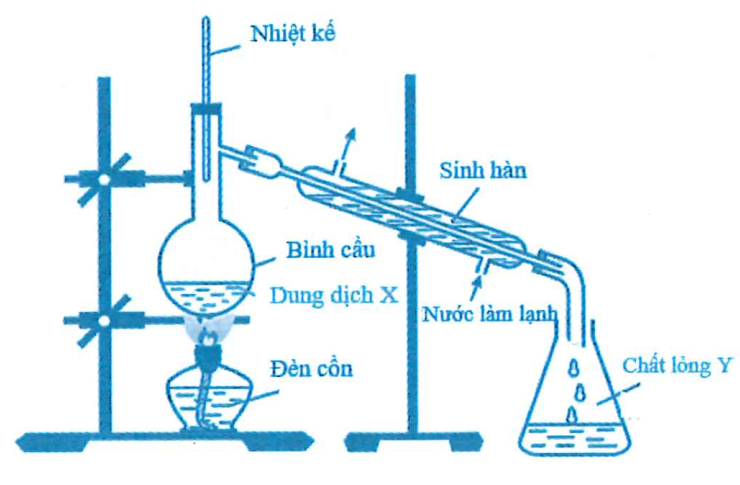
Trong thí nghiệm trên, xảy ra phản ứng hóa học nào sau đây?
 Xem đáp án
Xem đáp án
Nhận thấy C2H4 là chất khí, C6H5NH3Cl dạng rắn nên sẽ không thu được bằng cách ngưng tụ loại C, B.
Chất trong bình cầu là chất lỏng mà C2H4 là chất khí loại A.
Chọn đáp án D.
Câu 30:
Cho các phương trình phản ứng hóa học sau:
(1) .
(2) .
Phát biểu nào sau đây về X và Y là đúng?
 Xem đáp án
Xem đáp án
Các phản ứng xảy ra:
(1)
(2)
Vậy X là KOH và Y là Na2CO3.
A. Sai, vì KOH không thỏa mãn.
B. Đúng, cả 2 chất đều tác dụng được với dung dịch Mg(NO3)2 tạo kết tủa:
C. Sai, vì Na2CO3 không hòa tan được Al.
D. Sai, vì Na2CO3 có phản ứng: .
Chọn đáp án B.
Câu 31:
Tiến hành thí nghiệm với bốn dung dịch muối X, Y, Z và T chứa trong các lọ riêng biệt, kết quả được ghi nhận ở bảng sau:
|
Chất Thuốc thử |
X |
Y |
Z |
T |
|
Dung dịch Ba(OH)2 |
Xuất hiện kết tủa |
Xuất hiện kết tủa |
Xuất hiện kết tủa, có bọt khí thoát ra |
Xuất hiện kết tủa, có bọt khí thoát ra |
|
Dung dịch H2SO4 loãng |
Xuất hiện kết tủa, có bọt khí thoát ra |
Có bọt khí thoát ra |
Không xảy ra phản ứng hóa học |
Có bọt khí thoát ra |
Các dung dịch X, Y, Z, T lần lượt là
 Xem đáp án
Xem đáp án
Cho dung dịch Ba(OH)2 vào T thấy xuất hiện kết tủa và có bọt khí thoát ra Loại đáp án A do Ba(OH)2 tác dụng với Fe(NO3)2 chỉ tạo kết tủa.
Cho dung dịch H2SO4 loãng vào X thấy xuất hiện kết tủa và có bọt khí thoát ra Loại đáp án B. Loại đáp án D do chỉ có bọt khí thoát ra.
- Vậy chỉ có đáp án C thỏa mãn, các dung dịch X, Y, Z, T lần lượt là Ca(HCO3)2, Fe(NO3)2, (NH4)2SO4, (NH4)2CO3.
Chọn đáp án C.
Câu 32:
Cho sơ đồ chuyển hóa sau:
Biết X, Y, Z, T, E đều là hợp chất của nitơ, Z là khí không màu, nặng hơn không khí. Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
Theo đầu bài, CH4N2O phải tác dụng với nước, đồng thời tạo ra chất hữu cơ X tác dụng với NaOH, nên dễ tháy CH4N2O là urê. Khi đó:
A. Đúng.
B. Đúng. NH3 khi tan trong nước, một phần nhỏ các phân tử amoniac kết hợp với ion H+ của nước tạo thành cation ( ) và giải phóng anion ( ). Ion làm cho dung dịch có tính bazơ Dung dịch amoniac làm cho quỳ tím hóa xanh, còn dung dịch phenolphtalein từ không màu chuyển thành hồng.
C. Đúng. Trong hợp chất HNO3, nguyên tử N có số oxi hóa cao nhất là +5 nên axit nitric có tính oxi hóa mạnh, tùy thuộc vào nồng độ của axit và độ mạnh yếu của chất khử mà HNO3 có thể bị khử đến các sản phẩm khác nhau như N2, NH4NO3, N2O, NO, NO2.
D. Sai.
Chọn đáp án D.
Câu 33:
Cho các phát biểu sau:
(1) Anđehit vừa có tính oxi hóa vừa có tính khử.
(2) Phenol tham gia phản ứng thế brom khó hơn benzen.
(3) Amin bậc 2 có lực bazơ mạnh hơn amin bậc 1.
(4) Chỉ dùng dung dịch KMnO4 có thể phân biệt được toluen, benzen và stiren.
(5) Anilin có tính bazơ nên dung dịch anilin trong nước làm quỳ tím hóa xanh.
(6) Trong công nghiệp, chất béo được dùng để sản xuất glixerol và xà phòng.
(7) Đun nóng axit axetic với ancol isoamylic trong H2SO4 đặc thu được sản phẩm có mùi chuối chín.
Số phát biểu luôn đúng là
 Xem đáp án
Xem đáp án
Các phát biểu đúng là: (1), (4), (6), (7).
Chọn đáp án D.
Câu 34:
Có 3 dung dịch riêng biệt: H2SO4 1M; KNO3 1M; HNO3 1M được đánh số ngẫu nhiên là (1), (2), (3). Tiến hành các thí nghiệm sau:
Trộn 5 ml dung dịch (1) với 5 ml dung dịch (2), thêm bột Cu dư, thu được V1 lít khí NO.
Trộn 5 ml dung dịch (1) với 5 ml dung dịch (3), thêm bột Cu dư, thu được 2V1 lít khí NO.
Trộn 5 ml dung dịch (2) với 5 ml dung dịch (3), thêm bột Cu dư, thu được V2 lít khí NO.
Biết các phản ứng xảy ra hoàn toàn, NO là sản phẩm khử duy nhất, các thể tích khí đo ở cùng điều kiện. So sánh nào sau đây đúng?
 Xem đáp án
Xem đáp án
Thí nghiệm 1:
Thí nghiệm 2:
Từ đó, dễ nhận thấy: Lượng H+ ở dung dịch (3) gấp đôi lượng H+ ở dung dịch (2).
Suy ra, (1) (2) (3) lần lượt là: KNO3, HNO3, H2SO4.
Xét phản ứng: . Kết hợp dữ kiện ở thí nghiệm (1) và (3), dễ thấy: .
Chọn đáp án C.
Câu 35:
Từ chất X (C10H10O4, chỉ có một loại nhóm chức) tiến hành các phản ứng (theo đúng tỉ lệ mol):
(a) .
(b) .
(c)
Biết MY < MZ < MT < 148, Y và Z là muối của axit cacboxylic. Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
- X có , X chỉ chứa 1 loại nhóm chức và có khả năng tác dụng với NaOH X chứa 2 nhóm (do trong X có 4 nguyên tử oxi).
- X tác dụng với NaOH theo tỉ lệ mol 1 : 3 đồng thời sau phản ứng thủy phân thu được H2O X có 1 nhóm gắn trực tiếp vào vòng benzen.
- Mặt khác, MY < MZ < MT < 148 X có CTCT thu gọn là hoặc .
- MY < MZ < MT Y: HCOONa; Z: CH3COONa; T: ; E: HCOOH.
- Ở phản ứng (c) sau phản ứng thu được 2 phân tử H2O nên F có CTCT thu gọn là (HCOO)2C2H4.
A. Sai. Các CTCT thỏa mãn X
X có 6 công thức cấu tạo thỏa mãn.
B. Đúng. F là (HCOO)2C2H4 Có chứa 6 nguyên tử hiđro trong phân tử.
C. Đúng. Đun Z (CH3COONa) với vôi tôi xút, thu được khí CH4 (M = 16) nhẹ hơn không khí.
D. Đúng. T có chứa nhóm –OH nên có khả năng tác dụng với Na giải phóng khí H2.
Chọn đáp án A.
Câu 36:
Tiến hành điện phân dung dịch chứa a mol CuSO4 và b mol NaCl bằng dòng điện một chiều có cường độ 2A (điện cực trơ, màng ngăn xốp, hiệu suất điện phân 100%, bỏ qua sự hòa tan của khí trong nước và sự bay hơi của nước). Gọi V là tổng thể tích khí (đktc) thoát ra ở cả hai điện cực. Quá trình điện phân được mô tả theo đồ thị sau:
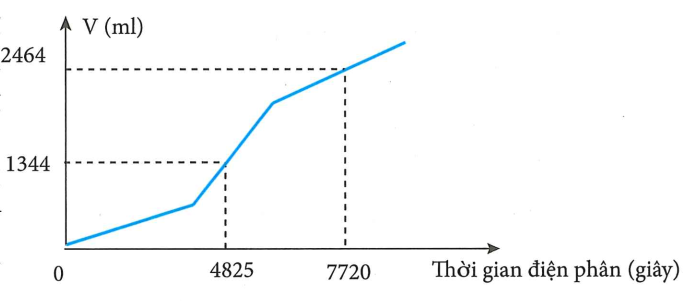
Tỉ lệ a : b là:
 Xem đáp án
Xem đáp án
Nhìn vào đồ thị, ta tấy quá trình điện phân gồm 3 giai đoạn.
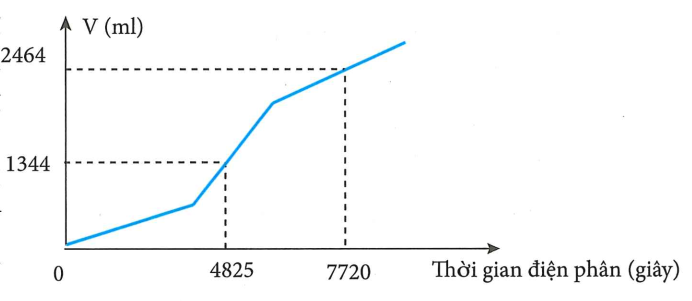
· Giai đoạn 1:
Catot: , Anot: .
2 mol e ứng với 1 mol khí sinh ra ở cả hai điện cực.
· Giai đoạn 2: Có hai trường hợp xảy ra.
+ Trường hợp 1: bị điện phân hết trước Cu2+.
Catot: ; Anot:
2 mol e ứng với 0,5 mol khí sinh ra ở cả hai điện cực.
+ Trường hợp 2: Cu2+ bị điện phân hết trước .
Catot: ; Anot:
2 mol e ứng với 2 mol khí sinh ra ở cả hai điện cực.
Nhìn vào đường gấp khúc của đồ thị, ta thấy đoạn hai dốc hơn đoạn một, do đó trường hợp xảy ra là trường hợp 2.
Số mol Cl2 thu được trong giai đoạn 1 là a. Gọi x là số mol Cl2 thu được từ khi Cu2+ bị điện phân hết cho đến thời điểm t1 = 4825s.
Ta có hệ:
· Giai đoạn 3:
Gọi y là số mol Cl2 thu được trong giai đoạn 2, z là số mol H2O bị điện phân cho đến thời điểm
Chọn đáp án B.
Câu 37:
Dẫn 4,48 lít CO (đktc) đi qua m gam hỗn hợp oxit nung nóng gồm MgO, Al2O3, Fe2O3 và CuO. Sau một thời gian, thu được hỗn hợp rắn X và hỗn hợp khí Y có tỉ khối so với H2 là 20,4. Cho X tan hoàn toàn trong dung dịch HCl (loãng), thu được dung dịch Z chỉ chứa (2m – 4,36) gam muối và thoát ra 1,792 lít (đktc) khí H2. Cho Z tác dụng hoàn toàn với dung dịch AgNO3 dư, thu được (5m + 9,08) gam kết tủa. Giá trị của m gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Xét phản ứng , cứ bao nhiêu mol CO mất đi thì có bấy nhiêu mol tạo thành, như vậy số mol khí không đổi.
Gọi
Sau khi phản ứng với AgNO3 dư, Fe có mức oxi hóa +3, không thay đổi so với hỗn hợp ban đầu, nên tổng số mol electron trao đổi của các chất oxi hóa phải bằng số mol electron trao đổi của các chất khử, cụ thể , trong đó CO là lượng đã phản ứng.
Gọi
Từ (1) và (2)
Câu 38:
Hỗn hợp X gồm một axit cacboxylic T (hai chức, mạch hở, có đồng phân hình học), hai ancol đơn chức cùng dãy đồng đẳng và một este hai chức tạo bởi T với hai ancol đó. Đốt cháy hoàn toàn a gam X, thu được 139,7 gam CO2. Mặt khác, đun nóng a gam X với 600 ml dung dịch KOH 2M, sau khi phản ứng xảy ra hoàn toàn, thêm tiếp 200 ml dung dịch HCl 1M để trung hòa vừa đủ lượng KOH dư, thu được dung dịch Y. Cô cạn Y, thu được m gam muối khan và 0,35 mol hỗn hợp hai ancol có phân tử khối trung bình nhỏ hơn 46. Giá trị của m gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Theo bài ra ta có:
.
Vì T là axit cacboxylic hai chức, mạch hở, có đồng phân hình học nên
Tiến hành quy đổi hỗn hợp X thành axit, ancol và H2O, ta được:
Theo BT.C:
Khi đó:
Câu 39:
Hòa tan hoàn toàn 43,56 gam hỗn hợp X gồm Mg, CuO, Fe3O4 và FeCO3 (trong đó nguyên tố oxi chiếm 22,04% về khối lượng) vào 960 ml dung dịch HNO3 2M, thu được dung dịch Y chỉ chứa muối và 2,688 lít (đktc) hỗn hợp khí Z gồm N2O, NO và CO2, có tỉ khối so với H2 là 18,5. Cho Y phản ứng tối đa với 1,77 lít dung dịch NaOH 1M (đun nóng), thu được kết tủa T. Nung T trong không khí đến khối lượng không đổi, thu được 48 gam chất rắn. Phần trăm khối lượng của CuO trong X có giá trị gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Ta có:
Quy đổi hỗn hợp X, ta có sơ đồ phản ứng sau:
Chọn đáp án D.
Câu 40:
Cho 2 peptit X, Y (MX < MY) và este Z (X, Y, Z đều mạch hở; X, Y đều được tạo từ Gly và Ala; Z có không quá 3 liên kết trong phân tử và được tạo từ phản ứng giữa axit cacboxylic và ancol). Đốt cháy hoàn toàn x mol X hoặc y mol Y hoặc z mol Z đều thu được hiệu số mol CO2 và H2O là 0,06 mol. Mặt khác, thủy phân hoàn toàn 42,34 gam hỗn hợp E gồm X (x mol), Y (y mol), Z (z mol) trong dung dịch KOH vừa đủ, cô cạn dung dịch sau phản ứng, thu được 1,86 gam ancol T và 72,32 gam hỗn hợp muối. Phần trăm khối lượng của Y trong E là
 Xem đáp án
Xem đáp án
Xét hai trường hợp
ü Trường hợp 1: Phân tử Z có 2 liên kết .
Ta có: Không có ancol T thỏa mãn.
ü Trường hợp 2: Phân tử Z có 3 liên kết
Ta có: T là C2H4(OH)2.
Z có dạng .
Quy đổi hỗn hợp E, ta có:
Dễ thấy CH2 không ảnh hưởng tới hiệu số mol CO2 và H2O, ta có hệ sau:
Xét phản ứng đốt cháy một peptit có k mắt xích, ta có:
Số mắt xích trung bình của peptit là:
Do X không thể là đipeptit
X là tripeptit Y là pentapeptit.
Tiến hành ghép CH2, ta có:
Chọn đáp án A.
