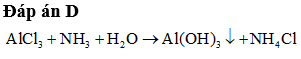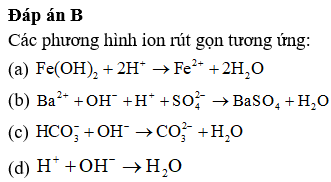Tuyển tập 20 đề thi thử THPTQG Hóa Học cực hay có lời giải chi tiết
Tuyển tập 20 đề thi thử THPTQG Hóa Học cực hay có lời giải chi tiết (Đề số 8)
-
2576 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Trong số các kim loại sau, cặp kim loại nào có nhiệt độ nóng chảy cao và thấp nhất:
 Xem đáp án
Xem đáp án
Đáp án A
Kim loại có nhiệt độ nóng chảy cao nhất là W, thấp nhất là Hg
Câu 2:
Trong các kim loại sau: Na, K, Mg, Al. Kim loại thuộc nhóm kim loại kiềm thổ là
 Xem đáp án
Xem đáp án
Đáp án C
Kim loại kiềm thổ (nhóm IIA) gồm: Be, Mg, Ca, Sr, Ba
Câu 3:
Nước ngầm thường chứa nhiều ion kim loại độc như Fe2+ dưới dạng muối sắt (II) hiđrocacbonat và sắt (II) hiđroxit. Nước sinh hoạt có chứa Fe2+ ảnh hưởng xấu đến sức khoẻ con người. Dùng phương pháp nào sau đây đơn giản nhất, tiện lợi nhất có thể áp dụng ở quy mô hộ gia đình để làm nước sạch:
 Xem đáp án
Xem đáp án
Đáp án A
Dùng giàn phun mưa để các ion Fe2+ tiếp xúc với không khí, các ion này sẽ bị oxi hóa thành ion Fe3+ không ảnh hưởng đến sức khỏe con người
Câu 4:
Este no, đơn chức, mạch hở có công thức phân tử là
 Xem đáp án
Xem đáp án
Đáp án B
Este no, đơn chức, mạch hở có công thức phân tử là CnH2nO2 với n 2
Câu 6:
Trong môi trường kiềm, protein có phản ứng màu biure với
 Xem đáp án
Xem đáp án
Đáp án C
Phản ứng màu biure xảy ra giữa các chất có từ 2 liên kết peptit trở lên với Cu(OH)2 trong môi trường kiềm
Câu 7:
Chất nào sau đây vừa phản ứng với dung dịch HCl, vừa phản ứng với dung dịch NaOH?
 Xem đáp án
Xem đáp án
Đáp án C
Al2O3 vừa phản ứng với dung dịch HCl, vừa phản ứng với dung dịch NaOH
Câu 8:
Công thức phân tử của kali đicromat là
 Xem đáp án
Xem đáp án
Đáp án A
Kali đicromat K2Cr2O7
Kali cromit KCrO2
Natri đicromat Na2Cr2O7
Kali cromat K2CrO4
Câu 9:
Polime nào sau đây chứa nguyên tố nito?
 Xem đáp án
Xem đáp án
Đáp án D
Tơ nilon-6 có chứa nguyên tố nitơ
Câu 10:
Dãy các kim loại đều có thể được điều chế bằng phương pháp điện phân dung dịch muối của chúng với điện cực trơ là
 Xem đáp án
Xem đáp án
Đáp án D
Nhận thấy Li, Al, Ca chỉ điều chế bằng phương pháp điện phân nóng chảy => loại A, B, C
Câu 11:
Trong công nghiệp, một lượng lớn chất béo dùng để sản xuất
 Xem đáp án
Xem đáp án
Đáp án A
Trong công nghiệp, một lượng lớn chất béo dừng để điều chế xà phòng, glixerol và chế biến thực phẩm
Câu 14:
Cho 300ml dung dịch AlCl3 1M tác dụng vói V lít dung dịch NaOH 1M, lượng kết tủa thu được là 15,6 gam. Giá trị lớn nhất của V là
 Xem đáp án
Xem đáp án
Đáp án A
n(Al3+) = 0,3; n(Al(OH)3) = 0,2
Giá trị V lớn nhất khi kết tủa khi NaOH hòa tan 1 phần kết tủa.
BTNT (Al): n(Al3+) = n(Al(OH)3) + n(AlO2-) => n(AlO2-) = 0,3 - 0,2 = 0,1.
BTĐT: n(AlO2-) = n(OH-) - 3n(Al3+) => n(OH-) = 0,1 + 3.0,3 = 1 mol =>V = 1 lít
Câu 17:
Cho 0,1 mol H2N-CH2-COOH tác dụng với 150 ml dung dịch HCl 2M, thu được dung dịch X. Cho dung dịch X tác dụng với dung dịch NaOH dư, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch chứa m gam muối. Giá frị của m là
 Xem đáp án
Xem đáp án
Đáp án D
Ta có : nHCl = 0,3 mol
Cho amino axit tác dụng với HCl rồi tác dụng với NaOH cũng như cho amino axit và HCl tác dụng với NaOH.
Do vậy số mol NaOH phản ứng là 0,4 mol.
Bảo toàn khối lượng: m = 0,1.75 + 0,3.36,5 + 0,4.40 - 0,4.18 = 27,25 gam
Câu 18:
Định nghĩa đồng đẳng nào sau đây là đúng ?
 Xem đáp án
Xem đáp án
Đáp án A
Đồng đẳng: là những hợp chất có thành phần phân tử hơn kém nhau một hay nhiều nhóm CH2 nhưng có tính chất hoá học tương tự nhau. Ví dụ như CH4, C2H6, C3H8...
Câu 20:
Nhận biết sự có mặt của đường glucozo trong nước tiểu, người ta có thể dùng thuốc thử nào trong các thuốc thử sau đây ?
 Xem đáp án
Xem đáp án
Đáp án D
Có thể dùng dung dịch AgNO3 để nhận biết sự có mặt của glucozơ
Câu 21:
Cho các hợp kim sau: Cu - Fe (I); Zn - Fe (II); Fe - C (III); Sn - Fe (IV). Khi tiếp xúc với dung dịch chất điện li thì các hợp kim mà trong đó Fe đều bị ăn mòn trước là
 Xem đáp án
Xem đáp án
Đáp án B
Sắt bị ăn mòn trước khi trong hợp kim sắt có tính khử mạnh hơn, do đó đáp án (I), (III), (IV).
Câu 22:
Số đồng phân amin bậc 2 của C4H11N là
 Xem đáp án
Xem đáp án
Đáp án A
Các đồng phân amin bậc 2 là:
(1) CH3 - NH - CH3 - CH3 - CH3
(2) CH3 - CH3 - NH - CH3 - CH3
(3) CH3 - CH(CH3) - NH - CH3
Câu 24:
Cho các chất sau:
CH3COOH (1), C2H5COOH (2), CH3COOCH3 (3), CH3CH2CH2OH (4).
Chiều tăng dần nhiệt độ sôi (từ trái qua phải) của các chất trên là
 Xem đáp án
Xem đáp án
Đáp án C
Nhiệt độ sôi phụ thuộc vào liên kết hiđro và phân tử khối.
- Dựa vào liên kết Hiđro, có lực liên kết H trong axit > ancol > este.
- Phân tử khối càng lớn thì nhiệt độ sôi càng tăng.
Nhiệt độ sôi theo chiều tăng dần: (3) < (4) < (1) < (2).
Câu 27:
Cho sơ đồ chuyến hóa sau:
C6H12O6 (glucozo) XY T C6H10O4
Nhận xét nào các chất X, Y, Z và T trong sơ đồ trên là đúng?
 Xem đáp án
Xem đáp án
Đáp án D
X là C2H5OH, Y là C2H4, T là HOCH2CH2OH
và sản phẩm cuối cùng là CH3COOCH2CH2OOCCH3.
Phát biểu đúng là T hòa tan được Cu(OH)2 ở điều kiện thường do tạo phức poliol
Câu 28:
Thực hiện các thí nghiệm sau:
(1) Cho dung dịch NaOH dư vào dung dịch Ca(HCO3)2.
(2) Cho Ca vào dung dịch Ba(HCO3)2.
(3) Cho Ba vào dung dịch H2SO4 loãng.
(4) Cho H2S vào dung dịch Fe2(SO4)3.
(5) Cho SO2 đến dư vào dung dịch H2S.
(6) Cho NaHCO3 vào dung dịch BaCl2.
(7) Cho dung dịch NaAlO2 dư vào dung dịch HCl.
Số trường hợp xuất hiện kết tủa khi kết thúc thí nghiệm là
 Xem đáp án
Xem đáp án
Đáp án C
Có 6 phản ứng thu được kết tủa
Câu 29:
Thực hiện các thí nghiệm sau:
(1) Sục khí CO2 dư vào dung dịch Ca(OH)2.
(2) Sục khí NH3 dư vào dung dịch AlCl3.
(3) Sục khi CO2 dư vào dung dịch NaAlO2.
(4) Cho dung dịch AgNO3 vào dung dịch FeCl3.
(5) Cho dung dịch HCl vào dung dịch K2SiO3.
(6) Cho ure vào dung dịch Ca(OH)2.
Sau khi kết thúc thí nghiệm, số trường hợp thu được kết tủa là
 Xem đáp án
Xem đáp án
Đáp án D
Xét từng thí nghiệm:
(1) không có kết tủa do CO2 dư hòa tan kết tủa CaCO3 tạo thành trước đó.
(2) tạo kết tủa Al(OH)3.
(3) tạo kết tủa Al(OH)3.
(4) tạo kết tủa AgCl.
(5) tạo kết tủa H2SiO3.
(6) tạo kết tủa CaCO3
Câu 30:
Cho các phát biểu sau:
(a) Cho dung dịch AgNO3 dư vào dung dịch FeCl2 sau phản ứng thu được hai chất kết tủa.
(b) Kim loại Cu tác dụng với dung dịch hỗn hợp NaNO3 và H2SO4 (loãng).
(c) Hỗn hợp Cu, Fe3O4 có số mol bằng nhau tan hết trong nước.
(d) Cho bột Cu vào lượng dư dung dịch FeCl3, thu được dung dịch chứa hai muối.
(e) Hỗn hợp Al và Na2O (tỉ lệ mol tương ứng là 2 :1) tan hoàn toàn trong nước dư.
(f) Cho Ba dư vào dung dịch Al2(SO4)3 sau phản ứng thu được hai chất kết tủa.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án D
Phát biểu đúng : (a), (b), (e).
Số phát biểu đúng: 3
Câu 33:
Cho các phát biểu sau:
(1) Ở người, nồng độ glucozơ trong máu được giữ ổn định ở mức 0,1%.
(2) Oxi hóa hoàn toàn glucozơ bằng hiđro (xúc tác Ni, t°) thu được sobitol.
(3) Tơ xenlulozơ axetat thuộc loại tơ hóa học.
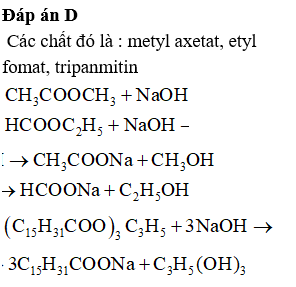
(4) Thủy phân este đơn chức trong môi trường bazơ luôn cho sản phẩm là muối và ancol.
(5) Số nguyên tử N có trong phân tử đipeptit Glu-Lys là 2.
(6) Tất cả các peptit đều có phản ứng màu biure.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án A
Xét từng phát biểu:
(1) Đúng.
(2) Sai, đây là phản ứng khử.
(3) Đúng.
(4) Sai, với trường hợp este phenol như CH3COOC6H5 thì sản phẩm là 2 muối.
(5) Sai, có 3 N.
(6) Sai, tripeptit trở lên mới có phản ứng màu biure.
Số phát biểu đúng là 2.
Câu 38:
Este X hai chức mạch hở (không có nhóm chức nào khác) được tạo thành từ ancol no, đơn chức và axit hai chức có một liên kết đôi C=C. Đốt cháy hoàn toàn m(g) X bằng O2 dư, hấp thụ hết sản phẩm cháy vào 200ml dung dịch Ba(OH)2 0,5M thu được 7,88g kết tủa và dung dịch Y, dung dịch Y có khối lượng tăng l,32g so với dung dịch bazơ đầu. Thêm NaOH vào Y thu được kết tủa. Mặt khác, xà phòng hóa m(g) X bằng Vml dứng dịch KOH 0,4M thu được dung dịch Z. Để dung hòa Z cần 200ml dung dịch H2SO4 0,2M thu được dung dịch G. Cô cạn G thu được 10,8g chất rắn khan. Số đồng phân mạch hở của X thỏa mãn tính chất trên là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 39:
Tiến hành thí nghiệm với các chất sau: glucozơ, anilin, fructozơ và phenol (C6H5OH). Kết quả được ghi ở bảng sau:
|
Thuốc thử |
X |
T |
Z |
Y |
(+): phản ứng (-): không phản ứng |
|
Nước Br2 |
Kết tủa |
Nhạt màu |
Kết tủa |
(-) |
|
|
Dung dịch AgNO3 trong NH3, đun nóng |
(-) |
Kết tủa |
(-) |
Kết tủa |
|
|
Dung dịch NaOH |
(-) |
(-) |
(+) |
(-) |
Các chất X, Y, Z, T trong bảng lần lượt là các chất:
 Xem đáp án
Xem đáp án
Đáp án B
Xét chất Y thấy anilin và phenol không tham gia phản ứng với dung dịch AgNO3 trong NH3, đun nóng => loại A, D.
Xét chất Z thấy anilin không tham gia phản ứng với NaOH =>loại C