Giải Sách bài tập Hoá học 10 Cánh diều Bài 3: Nguyên tố hóa học
Với giải sách bài tập Hoá học 10 Bài 3: Nguyên tố hóa học Cánh diều hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập trong SBT Hoá học 10 Bài 3
Giải sách bài tập Hóa học lớp 10 Bài 3: Nguyên tố hóa học
Bài 3.1 trang 7 SBT Hóa học 10: Đồng vị là những nguyên tử của cùng một nguyên tố hóa học, nhưng khác nhau về
A. tính chất hóa học.
B. khối lượng nguyên tử.
C. số proton.
D. số electron.
Lời giải:
Đáp án đúng là: B
Đồng vị là những nguyên tử của cùng một nguyên tố hóa học, nhưng khác nhau về khối lượng nguyên tử.
Bài 3.2 trang 7 SBT Hóa học 10: Trong tự nhiên, hydrogen có ba đồng vị (). Nguyên tử khối trung bình của hydrogen bằng 1,008. Hãy cho biết đồng vị nào của hydrogen chiếm tỉ lệ nhiều nhất trong tự nhiên.
A.
B.
C.
D. Không thể xác định được.
Lời giải:
Đáp án đúng là: A
Gọi x, y, z lần lượt là % số nguyên tử của mỗi đồng vị . Ta có công thức tính nguyên tử khối trung bình:
Do nguyên tử khối trung bình của hydrogen bằng 1,008 ≈ 1 nên đồng vị chiếm tỉ lệ phần trăm số nguyên tử nhiều nhất trong tự nhiên.
Bài 3.3 trang 7 SBT Hóa học 10: Hãy nối các mô tả trong cột A với các kí hiệu đồng vị trong cột B cho phù hợp.
|
Cột A |
Cột B |
|
a) Một đồng vị đồng có 34 neutron. |
|
|
b) Một đồng vị đồng có 36 neutron. |
|
|
c) Một đồng vị potassium có 21 neutron. |
|
|
d) Một đồng vị argon có 22 neutron. |
|
|
|
|
Lời giải:
a – 2; b – 1; c – 4; d – 3
Giải thích:
có số neutron bằng: 65 – 29 = 36.
có số neutron bằng: 63 – 29 = 34.
có số neutron bằng: 40 – 18 = 22.
có số neutron bằng: 40 – 19 = 21.
là kí hiệu hóa học sai vì K có số proton là 19.
Bài 3.4 trang 8 SBT Hóa học 10: Cặp nguyên tử nào sau đây có cùng số neutron?
A. và
B. và
C. và
D. và
Lời giải:
Đáp án đúng là: A
và có cùng số neutron là 6.
Bài 3.5 trang 8 SBT Hóa học 10: Deuterium (D) là một đồng vị của hydrogen, được ứng dụng trong các lĩnh vực hạt nhân. Ion nào sau đây có số electron nhiều hơn số proton và số proton nhiều hơn số neutron (Biết H = , D = , O = )?
A. D-.
B. H3O+.
C. OD-.
D. OH-.
Lời giải:
Đáp án đúng là: D
|
|
Số electron |
Số proton |
Số neutron |
|
D- |
1 + 1 = 2 |
1 |
1 |
|
H3O+ |
3 × 1 + 8 – 1 = 10 |
3 × 1 + 8 = 11 |
3 × 0 + 8 = 8 |
|
OD- |
8 + 1 + 1 = 10 |
8 + 1 = 9 |
8 + 1 = 9 |
|
OH- |
8 + 1 + 1 = 10 |
8 + 1 = 9 |
8 + 0 = 8 |
Bài 3.6 trang 8 SBT Hóa học 10: Phổ khối lượng của một mẫu lithium cho thấy nó chứa hai đồng vị là 6Li và 7Li với tỉ lệ phần trăm số nguyên tử của mỗi đồng vị lần lượt là 7,42% và 92,58%. Nguyên tử khối trung bình của mẫu lithium này (kết quả tính đến hai chữ số thập phân) là
A. 6,07.
B. 6,50.
C. 6,90.
D. 6,93.
Lời giải:
Đáp án đúng là: D
Nguyên tử khối trung bình của mẫu lithium này (kết quả tính đến hai chữ số thập phân) là:
Bài 3.7 trang 8 SBT Hóa học 10: Neon có ba đồng vị bền trong tự nhiên. Tỉ lệ phần trăm số nguyên tử mỗi đồng vị được thể hiện trong bảng sau:
|
Số khối |
A |
21 |
22 |
|
Tỉ lệ (%) |
90,9 |
0,3 |
8,8 |
Biết rằng nguyên tử khối trung bình của Ne là 20,18. Giá trị số khối A của đồng vị đầu tiên là
A. 19,00.
B. 20,00.
C. 20,01.
D. Không xác định được.
Lời giải:
Đáp án đúng là: B
Áp dụng công thức tính nguyên tử khối trung bình có:
Bài 3.8 trang 8 SBT Hóa học 10: Trong tự nhiên, carbon có hai đồng vị bền là 12C và 13C; oxygen có ba đồng vị bền là 16O; 17O và 18O. Số lượng tối đa loại phân tử CO2 có thể tạo ra từ các đồng vị này là
A. 6.
B. 9.
C. 12.
D. Vô số.
Lời giải:
Đáp án đúng là: C
Các loại phân tử CO2 có thể tạo ra từ các đồng vị này là:
16O 12C 16O; 16O 12C 17O; 16O 12C 18O; 17O 12C 18O; 18O 12C 18O; 17O 12C 17O;
16O 13C 16O; 16O 13C 17O; 16O 13C 18O; 17O 13C 18O; 18O 13C 18O; 17O 13C 17O;
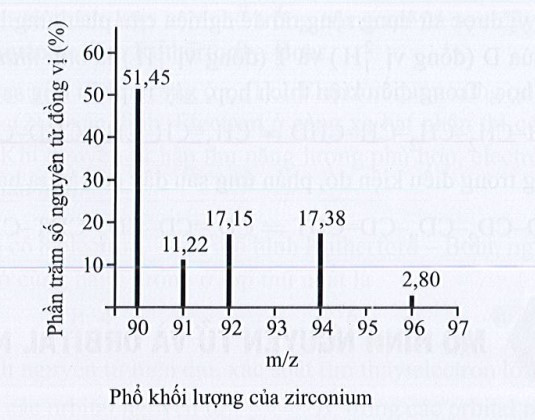
Bài 3.9 trang 8 SBT Hóa học 10: Phổ khối lượng của zirconium được biểu diễn như hình sau đây (điện tích z của các đồng vị zirconium đều bằng 1+).
Số lượng đồng vị bền và nguyên tử khối trung bình của zirconium là
A. 5 đồng vị, nguyên tử khối trung bình bằng 92,60.
B. 5 đồng vị, nguyên tử khối trung bình bằng 91,32.
C. 4 đồng vị, nguyên tử khối trung bình bằng 91,18.
D. 4 đồng vị, nguyên tử khối trung bình bằng 92,00.
Lời giải:
Đáp án đúng là: B
Quan sát phổ khối lượng của zirconium xác định được nguyên tố này có 5 đồng vị.
Nguyên tử khối trung bình của zirconium:
Bài 3.10* trang 9 SBT Hóa học 10: Bạc có hai đồng vị bền trong tự nhiên: 107Ag có hàm lượng tương đối là 51,8%; 109Ag có hàm lượng tương đối là 48,2%. Hãy vẽ phổ khối lượng của bạc và tính nguyên tử khối trung bình của Ag.
Lời giải:
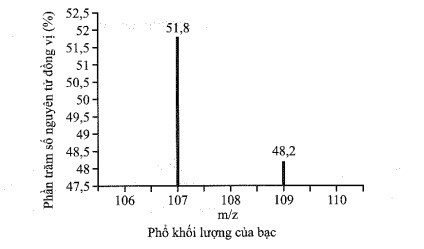
Nguyên tử khối trung bình của Ag là:
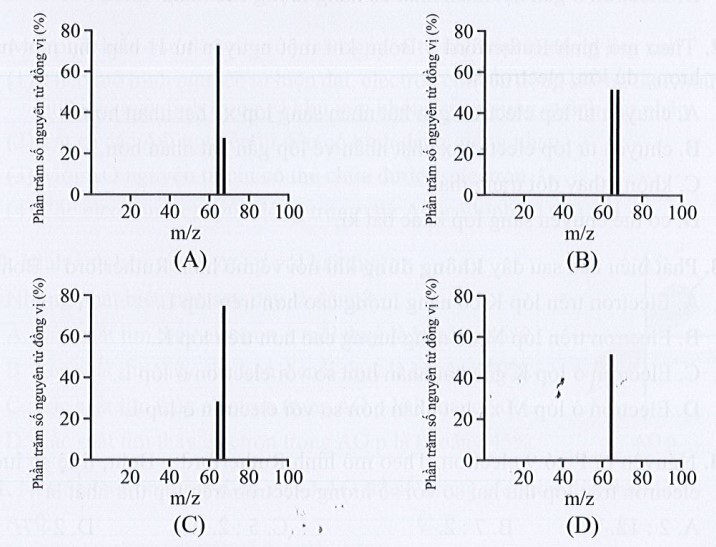
Bài 3.11* trang 9 SBT Hóa học 10: Đồng có hai đồng vị bền trong tự nhiên là 63Cu và 65Cu. Nguyên tử khối trung bình của đồng là 63,55 (điện tích z của các ion đồng vị đồng đều bằng 1+). Hình vẽ phổ khối nào dưới đây là đúng?
Lời giải:
Đáp án đúng là: A
Gọi % số nguyên tử của mỗi đồng vị 63Cu và 65Cu lần lượt là x và y (%).
Theo bài ra, ta có hệ phương trình:
Hình vẽ phổ khối đúng là: A
Bài 3.12* trang 10 SBT Hóa học 10: Đồng vị được sử dụng rộng rãi để nghiên cứu phản ứng hóa học. Cho biết vai trò của D (đồng vị ) và T (đồng vị ) là như nhau trong các phản ứng hóa học. Trong điều kiện thích hợp, xảy ra phản ứng sau:
CH2 = CH – CH2 – CH2 – CH = CHD ⇌ CH2 = CH – CH2 – CHD – CH = CH2 (1)
Vậy cũng trong điều kiện đó, phản ứng sau đây có xảy ra không?
CD2 = CD – CD2 – CD2 – CD = CDT ⇌ CD2 = CD – CD2 – CDT – CD = CD2 (2)
Lời giải:
Phản ứng (2) có xảy ra bởi vì phản ứng (1) xảy ra; vai trò của D và T là như nhau.
Bài viết liên quan
- Chủ đề 7: Nguyên tố nhóm VIIA (nhóm halogen)
- Giải Sách bài tập Hoá học 10 Cánh diều Bài 2. Thành phần của nguyên tử
- Giải Sách bài tập Hoá học 10 Cánh diều Bài 4: Cấu trúc lớp vỏ electron của nguyên tử
- Giải Sách bài tập Hoá học 10 Cánh diều Bài 5: Lớp, phân lớp và cấu hình electron
- Giải Sách bài tập Hoá học 10 Cánh diều Bài 6: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
